CHO(Chinese Hamster Ovary,中国仓鼠卵巢)细胞遗传背景清楚,内源蛋白分泌少,有利于外源蛋白的分离纯化,可以在优化的条件下进行大规模培养,已广泛应用于重组蛋白、抗体药物的大规模生产。
安必奇在稳定细胞系开发方向拥有丰富的经验,拥有稳定高产的CHO细胞株构建平台,我们的细胞库设施包括一个专用ISO7级制造套件,多个ISO5级工作空间和ISO7级和ISO8级支持室。从上游序列优化、载体构建,到细胞株构建,再到细胞株优化及质控检测,整个技术体系成熟,仪器设备齐全,能够快速助力于重组蛋白、抗体药物从研发到cGMP工业生产。基于多年的经验和创新,安必奇生物科技致力于为科研机构和药企提供稳定高产的CHO细胞株构建服务,为您提供稳定性良好、高产量、高质量、合规、快速的生产用细胞株。
服务范围
提供双特异性抗体、单抗等CHO细胞株开发服务;
提供激素、蛋白酶、细胞因子、凝血因子、Fc融合蛋白等CHO细胞株开发服务;
提供系统全面的表达产物质控、稳定性评估;
提供个性化培养基优化服务。
服务流程
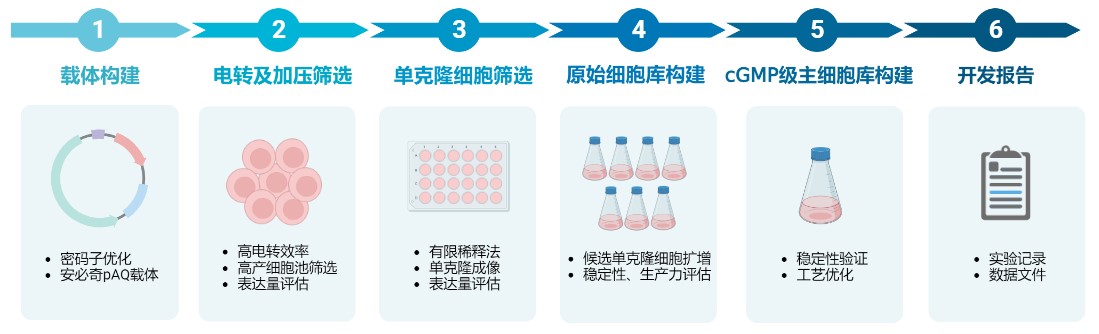
服务特色
稳定:基于多重筛选体系,1000+克隆逐步淘汰筛选,稳定传代30代以上
高产:已开发有成熟的、cGMP制造稳健的CHO K1-GS细胞系,具有高密度、高产量、适应大规模生产的独特优势,单克隆抗体生产可优化至6-8 g/L稳定表达
高质:系统全面的表达产物质控、稳定性评估
快速:筛选高产细胞株,周期12-16周
合规:细胞符合cGMP规范,有商业化授权,完善的技术转移流程,确保工艺的成功转移
案例展示
检测分析数据
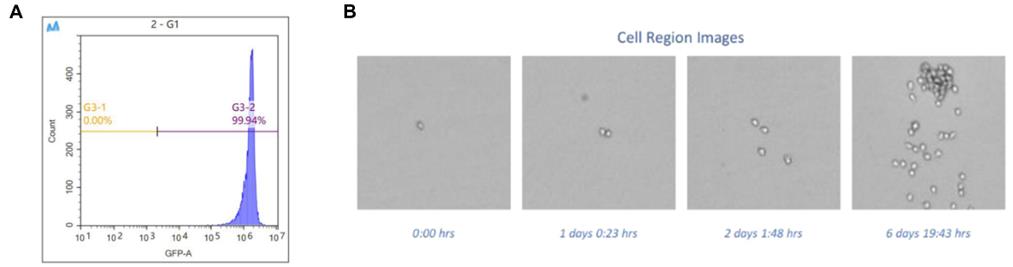 图1. A: CHO细胞株GFP表达FACS鉴定结果; B: 单克隆细胞筛选
图1. A: CHO细胞株GFP表达FACS鉴定结果; B: 单克隆细胞筛选
生产力数据
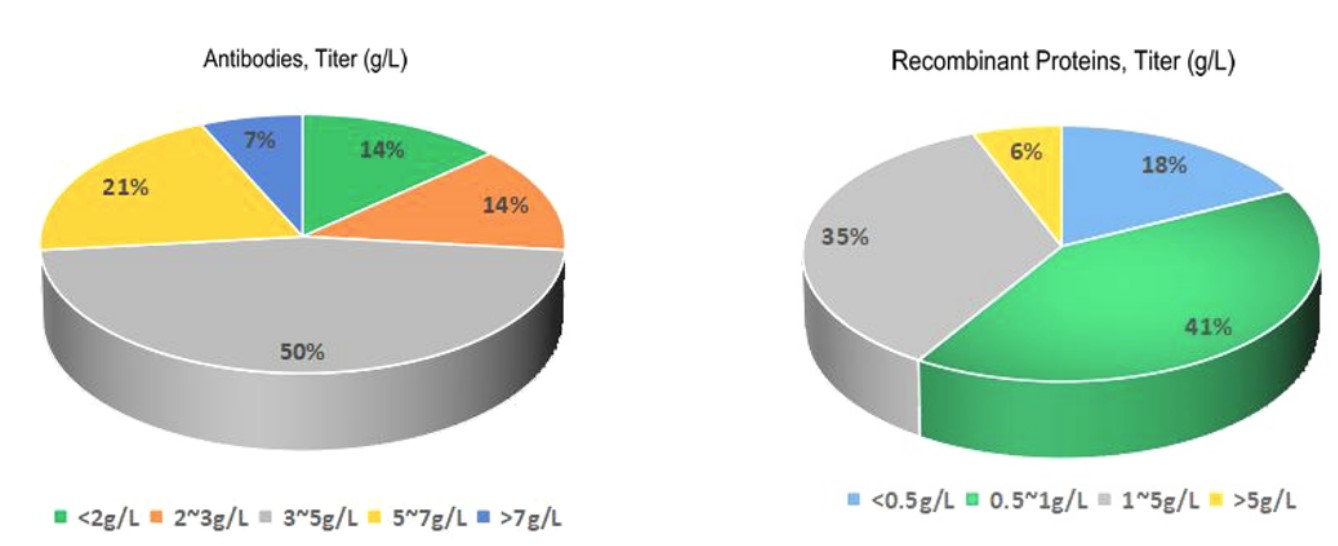 图2. CHO稳定细胞株具有良好的生产能力
图2. CHO稳定细胞株具有良好的生产能力
质量分析数据
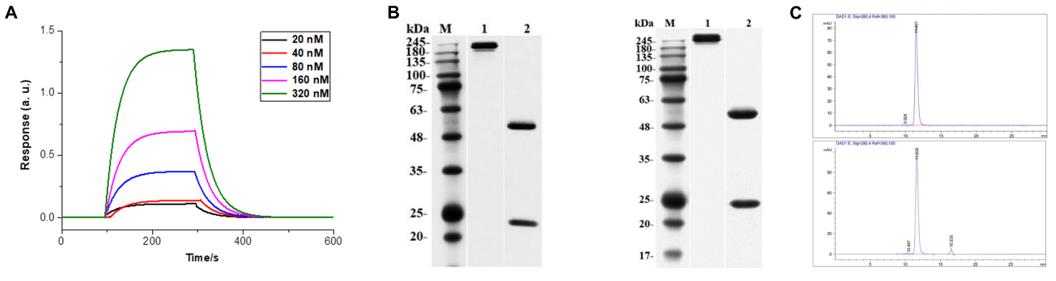 图3. A: Biacore 3000检测抗体亲和力; B: PAGE检测抗体纯度; C: HPLC检测抗体纯度
图3. A: Biacore 3000检测抗体亲和力; B: PAGE检测抗体纯度; C: HPLC检测抗体纯度
主要仪器设备展示

符合FDA, EMA, NMPA, cGMP要求;
具有成熟的GMP管理体系,严格遵循中国现行《药品生产质量管理规范》,采用原细胞库、主细胞库和工作细胞库三级细胞库管理模式,严格遵循《中国药典》对细胞库管理的详细规定;
具有先进的工艺控制水平及全面的质量控制和严格的产品放行流程。
交付内容
| 客户提供 | 交付物 | 周期 |
| 基因序列或质粒 | 高表达细胞池(1-5个) | 6-7周 |
| 基因序列或质粒 | 单克隆细胞株(3-6株) | 7-8周 |
| 基因序列或质粒 | 主细胞库 | 4周 |
| 基因序列或质粒 | 工作细胞库 | 4周 |
| 基因序列或质粒 | 细胞库稳定性分析(60-90代) | 10-13周 |
| 基因序列或质粒 | 纯化蛋白 | 4-10周 |
| 基因序列或质粒 | 纯化抗体 | 4-10周 |








