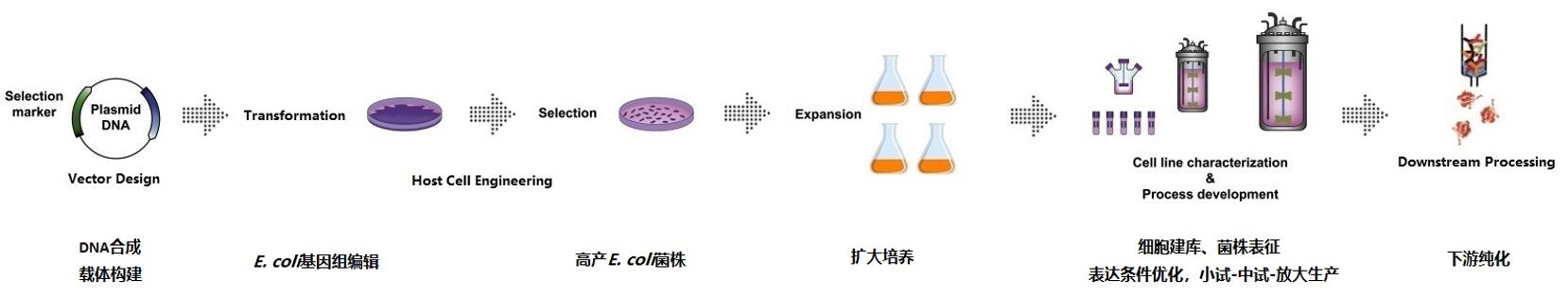
原核发酵应用于许多工业环境,包括生物制药、食品和饲料、化学品和生物燃料的制造。在生物制药行业,原核微生物是生产质粒、蛋白质、肽和小分子等治疗药物的工具。其中,大肠杆菌表达系统是经济实用的原核表达系统,具有遗传背景清楚、易于培养和控制、转化操作简单、表达水平高、成本低、周期短等优点。

图1 大肠杆菌工程菌商业化生产目标产物
服务项目
▪ 菌株构建
安必奇提供大肠杆菌基因工程菌株的定制化构建服务,得到的高产菌株易于进行工业化发酵,生产能力强,可以降低生产成本,提高经济效益。


▪ 发酵优化
发酵条件的优化(培养基及补料优化,溶氧量、温度、pH值控制)
大规模发酵生产
▪ 纯化工艺优化
通过疏水、亲和、凝胶过滤色谱、离子交换等纯化方式可获得纯度大于95%的目标蛋白。


▪ 冻干工艺优化
冻干过程包括三个阶段:(1)冷冻阶段,(2)初级干燥阶段和(3)二次干燥阶段。对多种条件下冷冻干燥试验过程中的关键参数进行优化,在不影响冻干制品质量的前提下(保证低的水分含量、具备优良的产品外观),缩短冻干工艺的周期。
平台设施

大肠杆菌发酵应用
大肠杆菌质粒生产
质粒是天然存在于细菌中的环状 DNA 分子,可以独立于基因组 DNA 进行复制。 质粒 DNA 在生物加工中发挥着重要作用,特别是在生物制药应用中,因为它涉及重组蛋白和病毒载体的生产。安必奇生物科技在利用大肠杆菌表达系统生产质粒DNA方面经验丰富,可为医药公司、工业客户提供从质粒构建、克隆筛选、菌种建库、工艺开发、非临床科研级质粒生产到GMP级别质粒生产的一站式个性化服务。
大肠杆菌重组蛋白表达生产
安必奇拥有多年的大肠杆菌重组蛋白表达经验,从蛋白性质分析,有很多蛋白及其结构域适合在大肠杆菌表达体系中表达。另外通过与 Sumo,Trx,GST 等标签融合也可以促进目的蛋白的表达及可溶表达。常见的表达产物包括毒性蛋白、生长因子、酶等,主要应用于作为抗原制备抗体、参与细胞实验与动物实验、测定蛋白酶活、研究蛋白相互作用(免疫共沉淀,GST pull down)、蛋白结晶结构研究、免疫组化实验等。
| 大肠杆菌蛋白表达项目分析 | |
| 蛋白特性 | 蛋白的分子量大小,蛋白来源/物种,是否为毒性蛋白,蛋白翻译后修饰程度, 蛋白结构复杂程度, 在细胞内外的定位等 |
| 蛋白表达系统 | 不同蛋白表达系统有不同的优势,如表达量高低,能否糖基化修饰等,结合蛋白应用并全面考虑,选择合适的蛋白表达系统 |
| 蛋白表达需求量 | 不同下游应用需求量有所区别,制备抗体需2 ~8mg,常规功能学研究10~200ug,细胞实验或药物研究则需更多 |
| 蛋白纯化处理 | 蛋白纯化标签主要有His、GST、SUMO、MBP等。His标签只有0.84kd,利于纯化且对蛋白无影响,可以保留;其他属于大标签,可以提高蛋白可溶性,但需要切除,否则会影响蛋白结构功能。 |
| 服务 | 服务内容 | 时间 | 交付结果 |
| 大肠杆菌蛋白表达 | 密码子优化 基因合成&载体构建 表达小试 放大表达&蛋白纯化 蛋白质检 内毒素去除服务(可选) | 4-6周 | 表达载体 3-5mg,> 90%纯度蛋白;工业级别的蛋白量(可选) 质检报告 项目流程报告 内毒素质检报告(可选) |
重组蛋白生产服务优势
成功交付上千种大肠杆菌体系重组表达蛋白,丰富的大肠杆菌重组表达资源,质粒(pET系列,pET28a,pET30a,pET43.1a等 ;pGEX4T-1,pBAD24,pGADT7,pQE-30等)、菌株齐全(BL21 (DE3)、OrigamiB(DE3)、Rosetta(DE3)、 BL21 CodonPlus(DE3)、ESL等),多种表达条件优化,增加可溶性蛋白表达量。
具备大肠杆菌表达可溶蛋白及体外复性蛋白 g 级生产能力。
大规模蛋白生产的平台,发酵罐、高压均质机等设备齐全。
大肠杆菌化工原料生产
大肠杆菌可以用于生产各种代谢产物和化学物质,如多肽、氨基酸、生物柴油、有机酸、多糖、抗生素等。大肠杆菌基因组改造可以发现新的特殊产物的基因,以及重要代谢过程和代谢产物生成相关的功能基因。安必奇生物提供定制化的大肠杆菌基因组编辑服务,优化代谢通路,提升代谢产物产量,实现工业化生产多种化工原料。
服务案例
案例1:
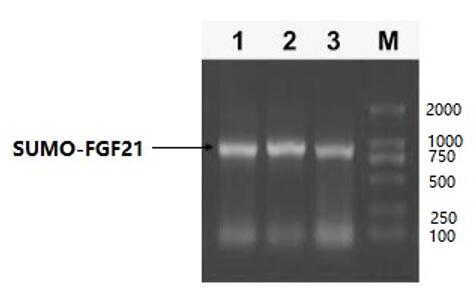
将重组质粒pET-SUMO-FGF21转化至大肠杆菌BL21 (DE3) 细胞中。5 mL Luria-Bertani (LB)培养基(1% 蛋白胨、1% 酵母提取物和0.5%氯化钠pH 7.0,含有100 μg/mL氨苄青霉素),37°C 、250 r/min摇瓶培养包含重组质粒的单克隆。过夜培养后,将 500 μL 培养物转移至 50 mL 新鲜 LB 培养基中进行指数生长。通过SDS-PAGE分离SUMO-FGF21,使用密度计扫描测量融合蛋白的产量,经过多个层析步骤回收高产率的重组质粒。
案例2:
根据客户的要求,利用大肠杆菌表达目的蛋白,并成功交付纯化的蛋白和CoA。 QC数据如下:
PCR验证

目的蛋白诱导表达
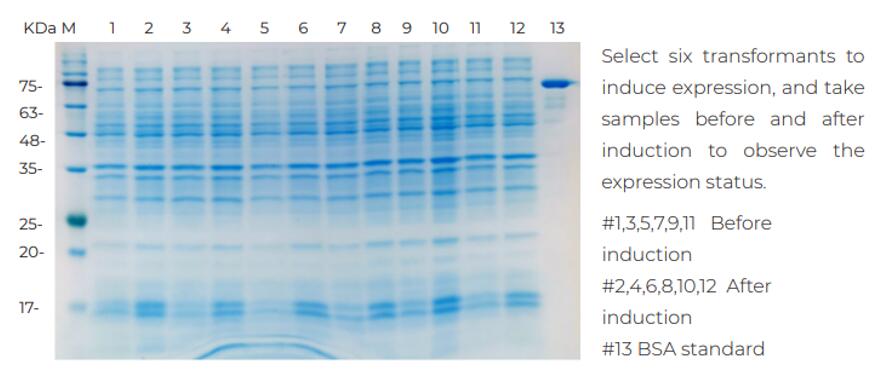
蛋白表达情况分析
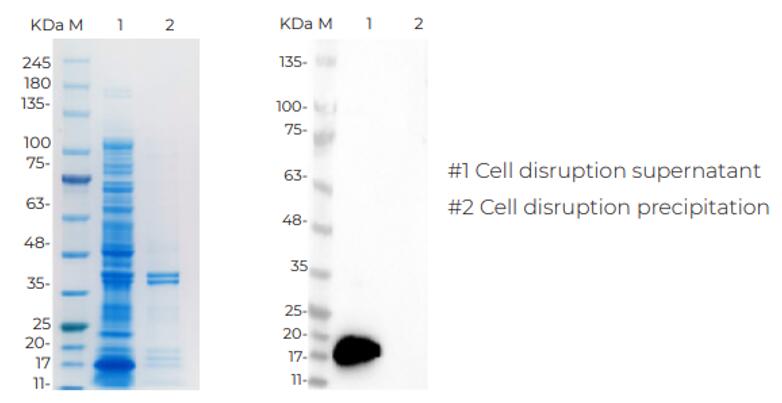
目的蛋白纯化
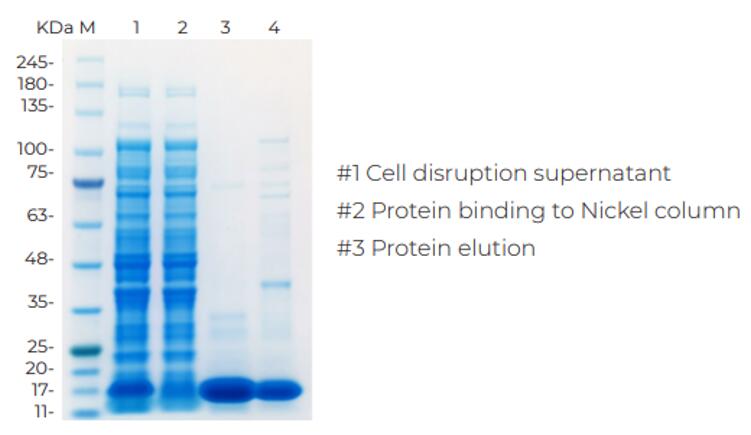
案例3:
在大肠杆菌内构建青蒿酸的生物合成途径,通过生物合成青蒿酸,再通过体外化学合成得到青蒿素, 几周内便可大量生产青蒿素。使用可控的 100 立方米工业发酵罐,可以替代 5 万亩的传统农业种植生产青蒿素,显著降低生产成本,具备低碳、绿色、环保的优势。

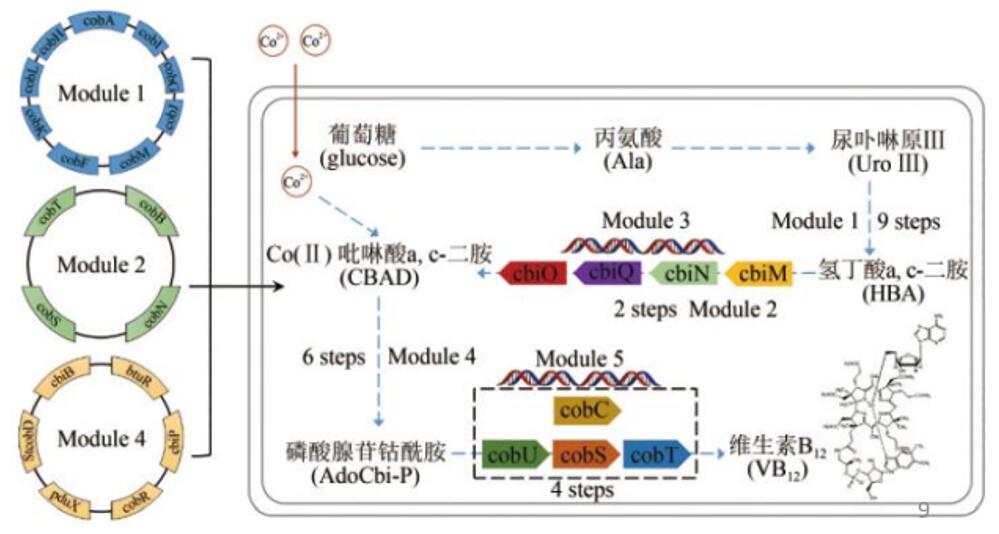
案例4:
在大肠杆菌中实现了VB12的从头合成,首先解析VB12好氧合成路径中钴螯合与腺苷钴啉醇酰胺磷酸的合成机理,将来源于5 种细菌中的28 个基因在大肠杆菌细胞中成功异源表达,并按其人工合成途径划分为5 个模块进行人工途径组装,最终实现VB12的从头合成,通过途径优化和发酵过程调控,产量达到307.00 μg/g 干细胞菌体,合成菌种发酵周期仅为工业生产菌株的1/10,具有工业应用前景。